 Für einen individuellen Ausdruck passen Sie bitte die
Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk, EU 2018, Lebensmittel - Arzneimittel

 Für einen individuellen Ausdruck passen Sie bitte die Für einen individuellen Ausdruck passen Sie bitte dieEinstellungen in der Druckvorschau Ihres Browsers an. Regelwerk, EU 2018, Lebensmittel - Arzneimittel |
 |
Durchführungsbeschluss (EU) 2018/133 der Kommission vom 24. Januar 2018 zur Änderung der Entscheidung 2008/911/EG zur Erstellung einer Liste pflanzlicher Stoffe, pflanzlicher Zubereitungen und Kombinationen davon zur Verwendung in traditionellen pflanzlichen Arzneimitteln
(Bekannt gegeben unter Aktenzeichen C(2018) 213)
(Text von Bedeutung für den EWR)
(ABl. Nr. L 22 vom 26.01.2018 S. 36)
Die Europäische Kommission -
gestützt auf den Vertrag über die Arbeitsweise der Europäischen Union,
gestützt auf die Richtlinie 2001/83/EG des Europäischen Parlaments und des Rates vom 6. November 2001 zur Schaffung eines Gemeinschaftskodexes für Humanarzneimittel 1, insbesondere auf Artikel 16f,
gestützt auf die Stellungnahme der Europäischen Arzneimittel-Agentur, die am 2. Februar 2016 vom Ausschuss für pflanzliche Arzneimittel abgegeben wurde,
in Erwägung nachstehender Gründe:
(1)Valeriana officinalis L. ist als pflanzlicher Stoff, pflanzliche Zubereitung oder eine Kombination davon im Sinne der Richtlinie 2001/83/EG zu betrachten und erfüllt die in der genannten Richtlinie festgelegten Bedingungen.
(2) Daher sollteValeriana officinalisL. in die mit der Entscheidung 2008/911/EG der Kommission 2 festgelegte Liste der pflanzlichen Stoffe, Zubereitungen und Kombinationen davon zur Verwendung in traditionellen pflanzlichen Arzneimitteln aufgenommen werden.
(3) Die Entscheidung 2008/911/EG sollte daher entsprechend geändert werden.
(4) Die im vorliegenden Beschluss vorgesehenen Maßnahmen entsprechen der Stellungnahme des Ständigen Ausschusses für Humanarzneimittel
- hat folgenden Beschluss erlassen:
Die Anhänge I und II der Entscheidung 2008/911/EG werden gemäß dem Anhang dieses Beschlusses geändert.
Dieser Beschluss ist an die Mitgliedstaaten gerichtet.
Brüssel, den 24. Januar 2018
2) Entscheidung 2008/911/EG der Kommission vom 21. November 2008 zur Erstellung einer Liste pflanzlicher Stoffe, pflanzlicher Zubereitungen und Kombinationen davon zur Verwendung in traditionellen pflanzlichen Arzneimitteln (ABl. Nr. L 328 vom 06.12.2008 S. 42).
| Anhang |
Die Entscheidung 2008/911/EG wird wie folgt geändert:
( 1) In Anhang I wird folgender Stoff nachThymus vulgaris L., Thymus zygis Loefl. ex L., aetheroleum eingefügt:
"Valeriana officinalis L.".
( 2) In Anhang II wird nach dem EINTRAG IN DER GEMEINSCHAFTSLISTE zuThymus vulgaris L.,Thymus zygis Loefl. ex L., aetheroleum Folgendes eingefügt:
"Eintrag in der Unionsliste zuValeriana Officinalis L.
Wissenschaftliche Bezeichnung der Pflanze
Valeriana officinalis L.
Botanische Familie
Valerianaceae
Gebräuchliche Bezeichnung des pflanzlichen Stoffs in allen EU-Amtssprachen
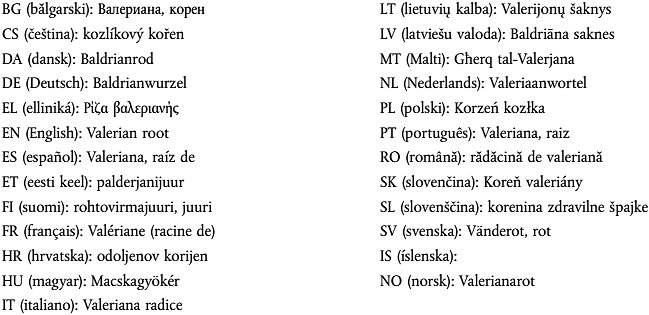
Pflanzliche Zubereitung(en)
Referenz der Monografie im Europäischen Arzneibuch
04:2017:0453
Anwendungsgebiete
Traditionelles pflanzliches Arzneimittel zur Linderung leichter Symptome von psychischem Stress und zur Unterstützung des Schlafes.
Das Produkt ist ein traditionelles pflanzliches Arzneimittel zur Verwendung für das spezifizierte Anwendungsgebiet ausschließlich aufgrund langjähriger Anwendung.
Art der Heiltradition
Europäisch
Spezifizierte Stärke
Siehe "Spezifizierte Dosierung"
Spezifizierte Dosierung
Jugendliche, Erwachsene und ältere Menschen
Zum Einnehmen
Zur Linderung leichter Symptome von psychischem Stress bis zu dreimal täglich.
(Stand: 11.03.2019)
Alle vollständigen Texte in der aktuellen Fassung im Jahresabonnement
Nutzungsgebühr: ab 105.- € netto
(derzeit ca. 7200 Titel s.Übersicht - keine Unterteilung in Fachbereiche)
Die Zugangskennung wird kurzfristig übermittelt
? Fragen ?
Abonnentenzugang/Volltextversion